


Injection d'insuline
Quelles options thérapeutiques
aujourd’hui ?



Injection d'insuline
Quelles options thérapeutiques aujourd’hui ?
Ces dernières années, « liberté », « qualité de vie » et « équilibre glycémique » ont été les maîtres-mots qui ont guidé les innovations scientifiques en matière d’injection d’insuline.
L’objectif guidant cette diversification : permettre à chacun de choisir une solution adaptée à sa vie et à sa situation avec les conseils du diabétologue.

L’histoire
de l’insuline*


1921
Découverte de l'insuline
La 1re injection d’insuline sur l’homme a eu lieu le 11 janvier 1922 et a permis de sauver Leonard Thompson, âgé alors de 14 ans et atteint d’un diabète et est tombé dans le coma. 1
1985
Le stylo injecteur :
une aide pour l’injection au quotidien
Deux types de stylos injecteurs sont disponibles : • Stylo pré-rempli, jetable après chaque utilisation. 2,3
• Stylo rechargeable, qui fonctionne avec des cartouches d’insuline pré-remplies contenant des doses variables à injecter. 2,3



Au quotidien
Une bonne utilisation nécessite un suivi précis des doses injectées, qui peuvent aller jusqu’à 5 injections par jour. 4
Les injections se font selon un schéma insulinique défini par le médecin et l’équipe médicale. 4

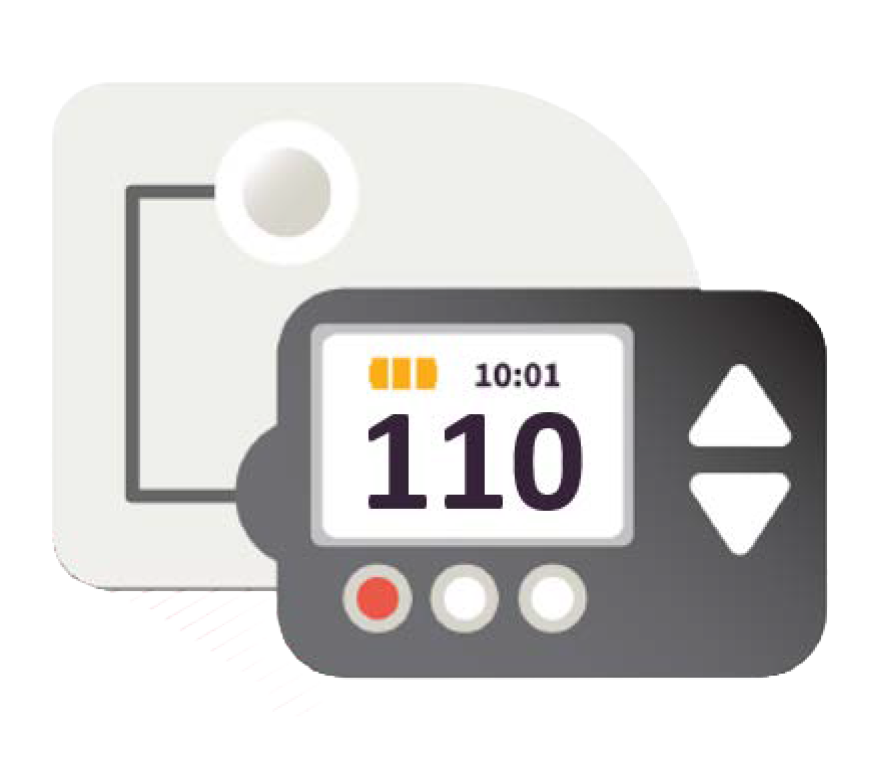
1990
La pompe à insuline :
action sur l’équilibre glycémique et diminution
du nombre d’injections
La pompe à insuline est reliée au corps via un dispositif de perfusion (tubulure et cathéter) qui permet de délivrer de l’insuline en continu. 5
La pompe est pré-programmée par l’équipe médicale et reproduit ce que l’organisme fait naturellement, en délivrant en continu de petites doses d’insuline rapide et des doses supplémentaires au moment des repas ou en cas d’hyperglycémie. 5

Au quotidien
La pompe à insuline se porte au quotidien, avec la possibilité de la déconnecter (par ex. lors de la douche). 5
Le cathéter peut être implanté à différents endroits du corps (abdomen, bras, cuisses, fesses), mais l’abdomen est privilégié pour que l’insuline diffuse le plus rapidement. 5,6
Ce dispositif offre de la flexibilité dans certaines situations du quotidien : en cas d’activité physique, le patient peut réduire son débit de base temporairement. Lors d’un en-cas imprévu, on peut rajouter une dose d’insuline sans avoir besoin de refaire une injection. 5,7
Une bonne utilisation nécessite une surveillance glycémique (glycémie capillaire ou lecteur flash) plusieurs fois par jour et le changement du cathéter tous les 2-3 jours. 5
2000
La pompe-patch à insuline :
l’arrivée de la pompe
patch à insuline
sans fil aux États-Unis



Au quotidien
Elle est étanche*, ce qui permet de se doucher ou de se baigner sans retirer le patch. Pour garantir l’efficacité du traitement, une surveillance régulière de la glycémie est indispensable, que ce soit par glycémie capillaire ou via un lecteur flash.
Le patch se remplace tous les trois jours.


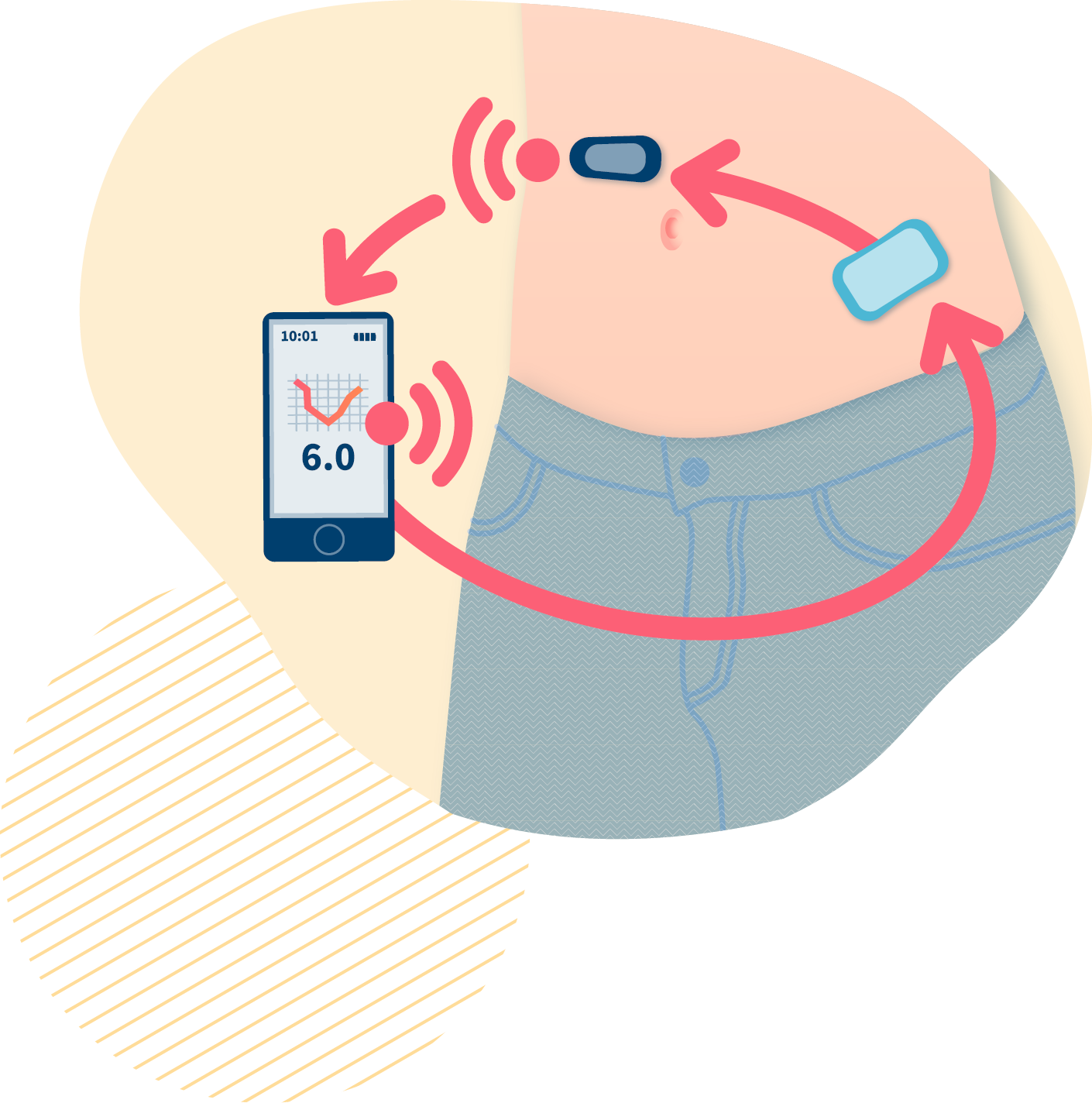
2010
L’arrivée du capteur de glucose en continu en France
L’arrivée du capteur de glucose en continu en France marque une avancée majeure dans la prise en charge du diabète. Ce dispositif permet aux patients de surveiller leur glycémie en temps réel.
Son utilisation peut contribuer à une meilleure compréhension des variations glycémiques au fil de la journée et à limiter les risques d’hypoglycémie et d’hyperglycémie. Certains patients peuvent y voir un moyen de gagner en autonomie dans la gestion de leur diabète.
Ces systèmes sont disponibles sur prescription médicale.


2023
Boucle fermée hybride :
un système automatisé pour mieux gérer le diabète
• Un patch ou une pompe à insuline filaire,
• un capteur mesurant en continu le taux de glucose,
• un algorithme qui analyse les données et ajuste automatiquement les doses d’insuline.
Le capteur transmet les données de glucose à la pompe via l’algorithme. Celui-ci prend en compte l’évolution du taux de glucose pour :
• réduire ou arrêter l’insuline en cas de risque d’hypoglycémie,
• augmenter la dose en cas d’hyperglycémie.
Ce système fonctionne en continu pour aider à maintenir un équilibre glycémique plus stable.
Le système est qualifié d’hybride car l’utilisateur doit intervenir dans certaines situations, notamment pour annoncer :
• la quantité de glucides consommés lors des repas,
• ainsi que les prévisions d’activité de la journée, comme l’activité physique.
Selon le modèle, ces actions peuvent être réalisées directement sur la pompe ou via une télécommande sans fil

Quels bénéfices pour le patient ?
- Réduction des variations glycémiques, notamment les hypoglycémies nocturnes. 10,11
- Amélioration de la qualité de vie, grâce à une charge mentale allégée et une surveillance continue. 12
- Plus de sérénité, notamment dans les moments où la vigilance est plus difficile (nuit, activité, déplacements). 12

Afin de choisir la solution la plus adaptée
à vos besoins, parlez-en à votre
professionnel de santé
* Le contenu présenté dans cette page n’a pas pour objectif d’effectuer une comparaison entre les différentes options thérapeutiques disponibles.
- Fédération Française des Diabétiques. Les 90 ans de la recherche de l’insuline. En ligne : https://www.federationdesdiabetiques.org/information/recherche-innovations-diabete/decouverte-insuline [consulté le 14/10/19].
- Dossier diabète ANSM. Disponible sur https://www.ansm.sante.fr/Dossiers/Diabete/Systemes-d-administration-d-insuline-et-precautions-d-emploi/(offset)/3. [Consulté le 25/04/2019].
- Verge D. Insulinothérapie : nouvelles molécules et voies d’administration. Médecine Sciences 2004; 20: 986-98.
- Fédération Française des Diabétiques. L’insuline. En ligne : https://www.federationdesdiabetiques.org/information/traitement-diabete/insuline [consulté le 14/10/19].
- Fédération Française des Diabétiques. La pompe à insuline. En ligne : https://www.federationdesdiabetiques.org/information/traitement-diabete/pompe-a-insuline [consulté le 14/10/19].
- Aide aux jeunes diabétiques. La pompe à insuline. En ligne : https://www.ajd-diabete.fr/le-diabete/tout-savoir-sur-le-diabete/la-pompe-a-insuline/ [Consulté le 09/03/2020].
- Pompe à insuline. En ligne : https://pompeainsuline.federationdesdiabetiques.org [consulté le 14/10/19].
- Schaepelynck P et al. Advances in pump technology: insulin patch pumps, combined pumps and glucose sensors, and implanted pumps. Diabetes & Metabolism 2011;37.
- Al-Tabakha MM, Arida AI. Recent Challenges in Insulin Delivery Systems: A Review. Indian J Pharm Sci 2008;70:278-86.
- Brown S. et al. Diabetes Care. 2021;44:1630-1640. Essai pivot prospectif mené auprès de 240 participants âgés de 14 à 70 ans atteints de DT1. L’étude comprenait une phase de traitement standard (TS) de 14 jours suivie d’une phase de 3 mois avec le système hybride en boucle fermée Omnipod 5.
- Sherr J. et al. Diabetes Care. 2022; 45:1907-1910. Essai prospectif mené auprès de 80 participants âgés de 2 à 5,9 ans atteints de DT1. L’étude comprenait une phase de traitement standard (TS) de 14 jours suivie d’une phase de 3 mois avec le système hybride en boucle fermée (HCL) Omnipod 5.
- Polonsky WH et al. Diabetes Res Clin Pract 2022;190:109998. Les adultes âgés de 18 à 70 ans (N=115) ont constaté une réduction du score de détresse alimentaire dans l’enquête T1-DDS après 3 mois d’utilisation de l’Omnipod 5 par rapport à la ligne de base : 1,73 contre 1,97, (P=0,0003), respectivement.


